くすりの臨床試験とは
けがをした時や病気になったとき、「くすり」を使って治療します。従来の「くすり」よりもっと副作用が少なく効果の高い「くすり」、新しく発見された病気を治療するための「くすり」、今まで治療することが難しかった病気を効果的に治療できる「くすり」など、次々に新しい「くすり」が生まれています。それらの「くすり」がどのように生まれるかご存知ですか?
病気やけがを治療するために欠かせない「くすり」や医療機器が世に出るためには 、ヒトに対する臨床試験を必ず実施しなければなりません。臨床試験とは、ヒトに対する有効性と安全性を確認するための試験です。新しい「くすり」を開発するために行われる臨床試験を治験といいます。治験を実施し、厚生労働省の認可を得なければ、薬は誕生できません。
臨床試験のルール
ヘルシンキ宣言
「医の倫理」について、世界医師会が採択した宣言です。周到な計画、自由意思による同意、患者の利益やプライバシーの保護など、臨床研究やヒトの組織を用いる研究で医師が守るべき倫理規定を定めています。これにより、被験者の利益は、科学や社会に対する寄与よりも優先されます。
臨床研究に関する倫理指針
厚生労働省が、臨床研究における被験者の保護のために、倫理的観点及び科学的観点から臨床研究に携わるすべての関係者が遵守すべき事項を定めたものです。
「医薬品の臨床試験の実施の基準」(GCP)
厚生労働省が治験のルールを定めたもので、治験は新薬の製造販売承認を目的に実施されるため、前述の「臨床研究に関する倫理指針」よりも厳しい運用となっていて、法的拘束力があります。参加する方の人権・安全が守られ、そして治験が倫理的かつ科学的に行われ、開発中のくすりの情報が正確に集められることを目的としている基準です。
治験(臨床試験)や臨床研究はこのような厳しいルールにのっとって実施されています。
くすりの開発プロセス
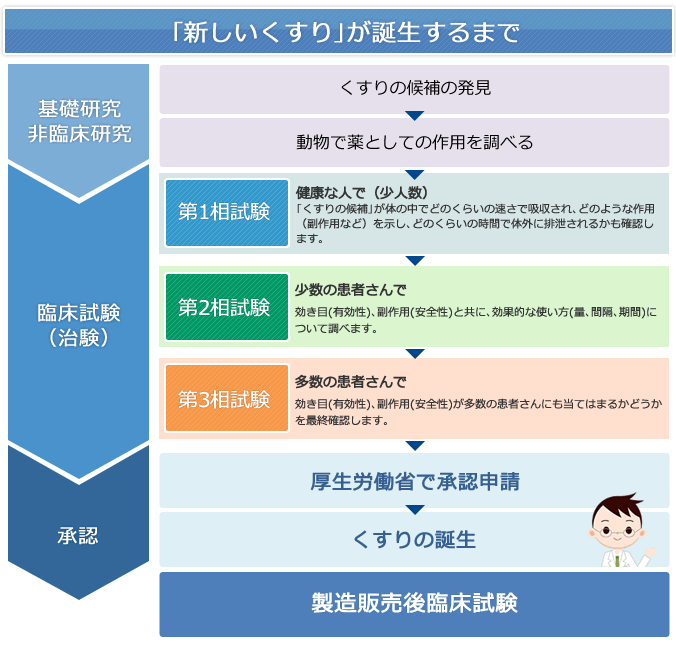

臨床試験の流れ
|
いよいよ臨床試験です。下記は実際の臨床試験の大まかな流れです。
|











